添加微信mede1917
或扫描二维码

添加微信mede1917
或扫描二维码

欢迎来到 Medebound 国际医疗平台
平安/泰康签约的优选服务机构
欢迎来到 Medebound 国际医疗平台
平安/泰康签约的优选服务机构


 美联医邦
美联医邦
文章类型: 公司合作互动
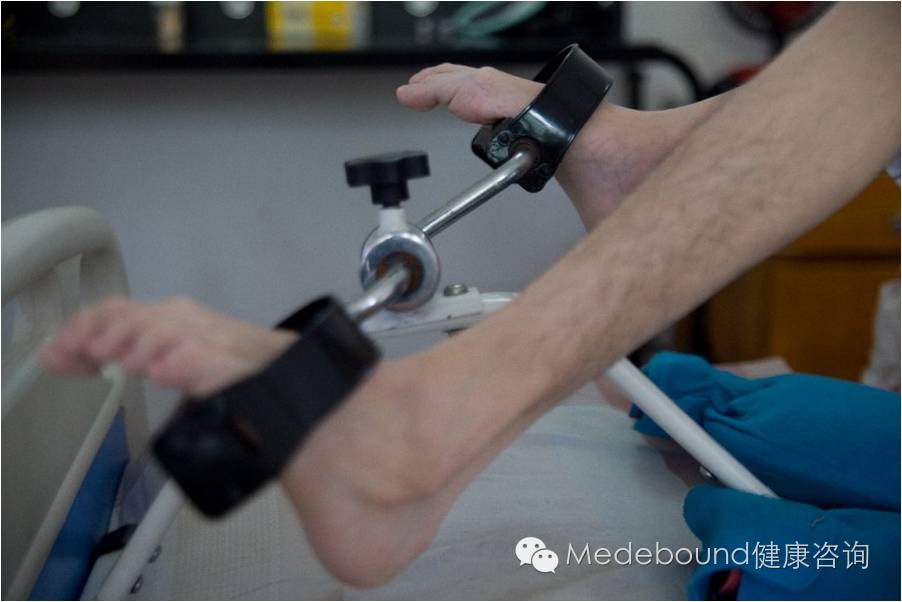
图一,庞贝氏患者在做腿部力量锻炼,长期卧床使他没有任何力气,需要凭借机械来锻炼
很多朋友并不知道什么是庞贝氏症,你们是幸运的。但只要在网上轻轻一搜,就会知道原来有这么多人都在经受着罕见病庞贝氏症的折磨,背负着一日万金的治疗费用。屡屡有家长为自己的庞贝氏子女在网上寻求着一丝生的希望。
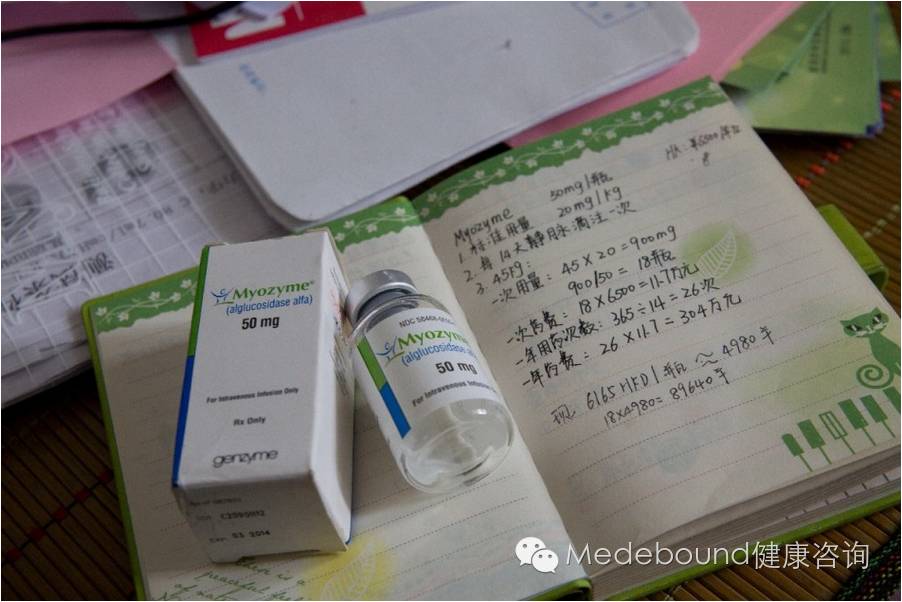
图二,妹妹为患病哥哥计算的药物用量,只有这种叫Myozyme的进口药物可以对这个疾病起到作用,由于并未获得国内销售许可,这个药物的购买和使用需要天价的成本。一年大概要花200万元人民币。
到底什么是庞贝氏症?

庞贝氏症又称为酸性α-葡萄糖苷酶缺乏症或糖原贮积症Ⅱ型(GSDⅡ)。由于溶酶体内缺乏酸性α-葡萄糖苷酶(acidalpha-glucosidase,GAA),使糖原及麦芽糖不能转化为葡萄糖而被利用,以致体内大量糖原在骨骼肌、心肌和平滑肌等组织细胞内聚积而致病。在北美及欧洲的发病率约为1:40,000,中国台湾发病率约为1:50,000。
根据发病年龄,一般将庞贝氏症分为两大类:婴儿型和晚发型。婴儿的疾病表现是最严重而且危及生命的,这个疾病的影响在出生的几个月内就出现,通常进展快速,主要临床表现为心肌肥厚,肝大,肌力和肌张力减退,一般一周岁内死于呼吸循环衰竭。晚发型庞贝氏症恶化较慢,而且不同病人间的差异很大,有些病人只有轻微的症状和稍许的肌肉无力;但是有些病人最后可能需要轮椅和呼吸器。一般而言,此型开始发作的年纪愈早,症状与恶化的情形愈严重。大部分的病人会因为呼吸逐渐恶化而缩短寿命。
为什么一日治疗需万金?
对于庞贝氏症,目前的治疗方法是酶替代疗法。通过静脉注射的方式定期向患者体内注射含有缺失的α-1,4-葡萄糖苷酶的药剂。酶替代疗法需终生进行,其成功与否取决于疾病阶段、疾病严重程度、酶治疗剂量、抗体产生等因素。2006年4月28日,由台湾中央研究院生物医学暨科学研究所所长陈垣崇及其所领导的研究团队,经过长达15年之研究,研发出全球第一个治疗庞贝氏症的药物《Myozyme》,并获欧盟医药品管理局(EMEA)及美国食品暨药物管理局(FDA)核准上市。然而该药在中国却尚未获的卫生部门批准,想要获得治疗,却是困难重重。庞贝氏药是一种孤儿药,在国内很难买到,由于这种罕见病药物品种少、价格昂贵,更不在医保目录中,因此许多患者家庭也难以承受。
庞贝氏孤儿药的新进展
法国制药巨头赛诺菲(Sanofi)旗下专科护理全球业务单元赛诺菲健赞(Sanofi Genzyme)近日宣布启动一项关键性III期临床研究(COMET),调查第二代酶替代疗法neoGAA治疗庞贝氏症(Pompe disease)的疗效和安全性。
该研究是一项开放标签、多中心、多国、剂量提升研究,在以前未接受治疗(初治)和已接受葡糖苷酶α治疗(经治)的晚发型庞贝氏症患者中开展,调查了neoGAA的安全性、耐受性、药代动力学、药效学、探索性疗效。研究中,可独立地不停歇行走距离≥50米且直立用力肺活量(FVC)≥50%基线的酸性α-葡萄糖苷酶缺陷成人患者,接受静脉输液neoGAA(5mg/kg,10mg/kg,20mg/kg,两周一次)治疗24周。初治组,10例接受治疗,其中9例完成了研究;经治组,14例接受治疗,其中12例完成了研究。数据显示,neoGAA在所有剂量水平的安全性和耐受性良好。研究中无患者死亡或危及生命的严重不良事件(SAEs)。
neoGAA是第二代阿葡糖苷酶α(alglucosidase alfa)酶替代疗法,阿葡糖苷酶α(品牌名:Lumizyme)是赛诺菲开发的第一代酶替代疗法,于2014年8月获FDA批准扩大适应症,用于全年龄段庞贝氏症(Pome)患者的治疗。临床前研究中,在降低组织糖原方面,neoGAA表现出约阿葡糖苷酶α5倍的功效。
希望与机会
美联医邦作为美国权威名医评鉴机构Castle Connolly Top Doctors独家战略合作伙伴,依托美国世界顶级前5%尖端医疗资源,不断为中国患者带来罕见病治疗领域最权威、最先进的医疗信息。我们致力于以互联网为中心的医患交流和远程咨询平台,对接全美上万名最顶尖TOP5%、跨72个专业领军医生资源。在此次人类与罕见病庞贝氏症的抗争中,美联医邦竭力为中国庞贝氏患者打开一条生命的绿色通道,提供去美国加州免费治疗一年的机会和平台,希望可以传达到需要帮助的患者家庭。
美国庞贝氏症临床试验要求
药品厂商:赛诺菲(Sanofi)
对照组: Sanofi的金标准药Myozyme(一年需用药费~120万全免)
试验组:Sanofi的疗效更好的新药 neoGAA (比Myozyme更好的药物,药费也全免)
两组都免费。临床实践一年,需要在加州待一年,每两周去一趟医院接受治疗。
试验阶段:III期
纳入标准:
病人已经确证患有任意组织来源的棉酚酶缺乏症以及/或者确证棉酚的基因突变
病人必须在进行任何与研究相关的程序之前,提供已经签字的知情同意书。 同意将一个合法的未成年病人纳入研究需要一个合法授权的监护人。 如果病人是合法的未成年人,那么知情同意书应当由父母或者合法的监护人签署并且获得病人的同意。
病人(如果病人是未成年人的话,还需病人的合法监护人)必须具备遵从临床方案的能力。病人如果是有生育能力的女性,必须在基线时妊娠测试显示阴性(β人体绒毛膜促性腺激素)
排除标准:
病人的年龄小于3岁
病人已经确定是庞贝氏症特异性心肌肥厚
病人依赖轮椅
病人不能在没有辅助设备的情况下连续走动40米(大约130英尺)
病人需要侵入式的机械通气(非侵入式的机械通气是准入的)
病人不能顺利的执行重复用力肺活量测试在直立位置,并达到期望值区间≥30%和≤85%
病人已经服用过糖苷酶-α治疗或者任何关于庞贝氏症的临床试验药物
病人以前使用过或者现在正在使用免疫耐受诱导治疗
所需花费:临床试验的活检和分子检测费用不需要患者支付,如果患者符合入组条件,他们所获得的治疗药物也将不收取任何费用。患者需要自己支付的费用,包括美联医邦国际专家初期会诊评估费用,医疗陪同和随访费用,旅途和住宿费用。临床试验以外,为了减轻患者的活检和治疗的副作用而采用其他检测、手术或药物所产生的费用。请拨打文末400电话发出申请。
为了爱,请转发给您周围可能需要帮助的孩子。
本文由美联医邦Medebound原创,欢迎转发,未经美联医邦允许,不得转载,违者必究。
部分美联医邦美国名医真实案例:
☞中国还原体肌病患儿获美国专家免费5+小时多学科会诊、免费食宿,感恩遇见美国最高政府卫生研究院
☞膀胱癌患者通过视频会诊中美两国三地联线哈佛名医,寻求治疗方案及临床试验建议
微信公众号:medebound

凭借我们30多年的美国医疗网络资源,您可以直接与美国医疗精英对话,在家中咨询美国顶级专家或国际会诊,不出国门获取先进治疗方案。
凭借我们30年的医疗网络资源,您可以直接与美国医疗精英对话。在家中咨询疑难疾病的专家,轻松了解治疗方案。
如需赴美就医或获取海外新药,我们为您一站式安排海外看病等服务。



服务优势
预约知名美国专家譬如安德森癌症医院和梅奥诊所,安排无忧出国看病行程,寻找全球新药新技术医生网络
我们与美国顶级1%的海外医疗医生网络,300+所美国权威医院和药房资源深度合作一站式海外诊疗我们的专属客服医学经理,为您免费咨询,最短时间获取预约优质医疗资源

Jason 王经理
医学客服经理/添加微信:Mede2018

Kiki 圆经理
医学客服经理/添加微信:mede1917
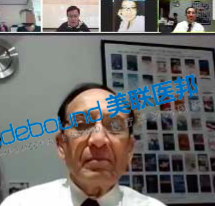
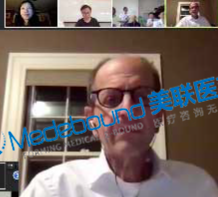
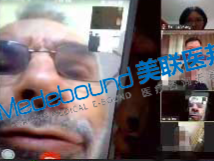

如果您和您的家人有任何医疗和新药需求,请欢迎随时联系我们。我们客服团队工作时间周一到周五早上9点到晚上8点,北京时间。
总部位于纽约,9年专注美国,是赴美就医服务细分领域的头部机构。 始终坚持精英式定制(非保姆式),获30+历史卡思克鲁力医生集团(全美TOP医生联盟)及股东战略产业投资,不涉及风险资本。 作为美国本土医疗资源提供商,美联医邦已与中国平安、泰康人寿、太平人寿等保险集团达成总对总合作。服务覆盖数百万保险客户。美国福布斯榜推荐和英文报道,直通全美前5%顶级专家网络。只精准对接全美72个专科排名TOP3医院,包括梅奥诊所、MD安德森、纪念斯隆-凯特琳癌症中心等百余家美国著名医疗机构。申请美国医院的折扣率10-30%,和美国医院议价能力高。3000+客户的信任选择,一切从用户角度出发,鼓励部分患者远程二诊/问诊拿方案在国内治疗,不过度宣传和劝退不必要的赴美看病。
了解更多美国美联医邦成都运营服务中心
Disclaimer 免责声明:
本文无意影响或改变您的主治医生提供的医疗服务。请不要在没有先咨询您的主治医疗服务提供者的情况下对您的治疗做出改变。本文不用于诊断或治疗疾病,也不影响治疗方案。美联医邦会尽最大努力编辑和更新本页面的信息,但是我们无法保证本页医药信息的精确性和完整性。
纽约总部:
260 Madison Ave 8th Floor #8001,New York, NY 10016
美联医邦Medebound成都运营服务中心:
成都市锦江区红星路一段35号A区1号楼605
(美)+1 917-342-2381
(中) +86 400-616-2591
support@medebound.com