T细胞需要两个信号才能完全激活。第一个信号来自T细胞受体(TCR)与抗原肽主要组织相容性复合物(MHC)的相互作用,该复合物给予免疫应答的特异性。为了完全激活,T细胞需要通过T细胞上的CD28和抗原呈递细胞(APC)上的B7-1和B7-2之间的相互作用发生的共刺激性抗原依赖性信号。
T细胞表达CTLA-4是防止免疫系统过度刺激的重要机制之一。CTLA-4与B7复合物的亲和力比CD28高100倍,并且这种相互作用导致对细胞的抑制。目前,CTLA-4抑制剂已被批准用于黑色素瘤。
免疫应答逃避的另一个重要机制是受PD-L1表达的调控。PD-L1与T细胞上的PD-1结合,出国看病服务机构了解到通过促进淋巴结中抗原特异性T细胞的凋亡并同时减少调节性T细胞(Tregs)中的细胞凋亡,从而启动双重抑制机制,调节性T细胞(Treg)具有抑制作用。相互作用发生后,PD-1在其两个胞内酪氨酸上磷酸化,并随后结合两种磷酸酶SHP-1和SHP-2。这两种磷酸酶可以结合到PD-1的基于免疫受体酪氨酸的抑制性基序(ITIM)和基于免疫受体酪氨酸的转换基序(ITSM),从而下调抗体-受体信号传导。当ITSM单独发生突变时,PD-1失去其抑制功能,使得该酪氨酸在PD-1抑制中起关键作用。PD-L1对B7-1的亲和力高于CD28,这进一步增加了抑制途径中的抑制作用。此外,PD-L2的表达仅限于APC和Th2细胞。因此,虽然PD-1也与PD-L2结合,但研究表明,与PD-L1抑制相比,抑制PD-L2不会产生有效的T细胞活性。
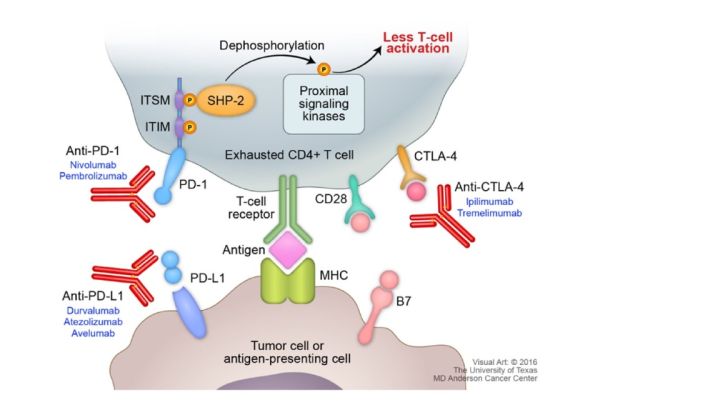
图片来源:MD Anderson Cancer Center
出国看病服务机构了解到,近年来的研究已经对减少抗肿瘤免疫应答的因素有了更清楚的认识,从而发现了几种能够用于免疫共刺激和抑制检查点途径的药物。介导肿瘤诱导的免疫抑制检查点分子的代表性例子就是程序性死亡-1(PD-1)。
从生理上来说,出国看病服务机构了解到PD-1 / PD-L1途径是机体需要在表达抗原的部位来控制炎症的程度,以确保正常组织免受损伤。在所有活化的T细胞表面都存在PD-1蛋白的显著表达。当T细胞识别靶细胞上MHC(主要组织相容性复合物)所表达的抗原时,就会产生炎性细胞因子,引发炎症过程。这些细胞因子导致组织中的PD-L1表达,激活T细胞上的PD-1蛋白从而导致免疫耐受。在某些肿瘤中,特别是在黑色素瘤中,这种保护性机制通过PD-L1的过表达而被扭曲,结果使得肿瘤逃避了机体的免疫应答。
在药理学上,PD-1/PD-L1抑制剂可以防止PD-1/PD-L1相互作用,从而促进阳性免疫应答以杀死肿瘤。尽管PD-1/PD-L1抑制剂作为抗癌药物具有明确的益处,但其应用的局限性在于它们的活性依赖于能够通过抗原呈递细胞(APCs)识别肿瘤的T细胞群的产生。如果这种T细胞群的产生遇阻,那么阻断PD-1 / PD-L1是无效的,因为缺乏免疫应答来有效杀伤肿瘤细胞。尽管肿瘤表达PD-L1可能暗示肿瘤可抑制免疫应答,并且因此可以作为临床获益的潜在生物标志物,但显然不是所有表达PD-L1的肿瘤都对PD-1/PD-L1抑制剂有反应。相反,有学者发现PD-L1阴性的肿瘤也可以对这些药物起反应。
在肿瘤微环境中,PD-1及其配体PD-L1通过使肿瘤逃避免疫监视在肿瘤的进展和存活中发挥重要作用。PD-1在各种免疫细胞上都有表达,如单核细胞、T细胞、B细胞、树突细胞和肿瘤浸润性淋巴细胞(TILs)。而PD-L1在肿瘤细胞和抗原呈递细胞(APC)中表达,并且PD-L1与T细胞的PD-1结合导致肿瘤中T细胞功能障碍、T细胞耗尽、T细胞中和以及白细胞介素-10(IL-10)的产生。因此,肿瘤过度表达PD-L1的目的就是要保护自身免受细胞毒性T细胞(CD8+)介导的细胞杀伤作用。
另一种相互作用的分子,如活化的T细胞和APC上表达的蛋白B7-1(CD80)与肿瘤细胞的PD-L1相互作用,引起效应T细胞活化的负调节。由于CD8+T细胞的耗尽,肿瘤细胞变得非常有侵袭性并分泌几种促炎细胞因子,如肿瘤坏死因子α(TNF-α)、白细胞介素-2(IL-2)和γ干扰素(IFN-γ)。
T细胞的另一种亚型,出国看病服务机构了解到如调节性T细胞(Treg, CD4+Foxp3+)通过维持其表面上的PD-1表达而产生高度免疫抑制的肿瘤环境。已经发现,在CD3和TGF-β存在的情况下,调节性T细胞的PD-1受体增加了幼稚CD4+T细胞向调节性T细胞的重新转化,从而减弱免疫应答。这种转化通过抑制雷帕霉素靶标(mTOR)-Akt信号级联反应来增加对CD4+T细胞的免疫抑制作用并增加调节性T细胞的表达。因此,PD-1表达的存在不仅抑制效应T细胞功能,还增加了免疫抑制调节性T细胞群的转化。
尽管PD-1在T细胞中被广泛研究,但其在B细胞中的功能也在肿瘤免疫抑制中起到了重要作用。已经发现在B细胞分化期间PD-1的表达受到高度调节,但是在pro-B细胞(成熟B细胞的早期阶段)中PD-1水平并不明显并且随着B细胞分化而增高。此外,PD-1活化的Toll样受体9(TLR9)激动剂可明显增强B细胞的成熟。现已发现抑制B细胞上的PD-1功能可增强抗原特异性抗体应答,表明PD-1在抑制B细胞介导的T细胞活化中发挥作用。
PD-1有两个结合配体,即PD-L1(B7-H1)和PD-L2(B7-DC),其中PD-L1负责肿瘤免疫调节。PD-1与PD-L1的结合亲和力是PD-1与PD-L2之间的亲和力的三倍。肿瘤细胞和造血细胞中的PD-L1表达通过刺激促炎细胞因子如IFN-γ和TNF-α来测定。虽然PD-L1在广泛的造血细胞和非造血细胞中表达,但在分泌IL-4和IFN-γ时PD-L2在巨噬细胞、树突细胞(DC)和肥大细胞中的表达受限。有研究发现PD-L2与巨噬细胞(M8)蛋白的排斥性引导分子B(RGMB)相互作用。目前有关PD-L2在癌症免疫抑制中的作用的资料还很少。
另一个重要的检查点分子CTLA4通过下调CD4+T效应细胞和增强调节性T细胞活性而广泛参与肿瘤的免疫逃避。CTLA-4是CD28(T细胞受体的共刺激因子)的同系物,出国看病服务机构了解到与APC的B7-1/2蛋白结合并确定T细胞是否会发生激活或抑制。目前认为与B7结合的CTLA-4产生T细胞抑制信号。因此,对PD-1/PD-L1和CTLA-4/B7轴的联合抑制已被确立为对各种恶性肿瘤患者有效的抗肿瘤治疗策略。肿瘤基质成分中的PD-L1,如成纤维细胞、细胞外基质(ECM)、肿瘤相关巨噬细胞(TAM)和骨髓衍生抑制细胞(MDSC),通过与PD-1相互作用使T细胞(CD8+)介导的癌细胞杀伤作用失活。
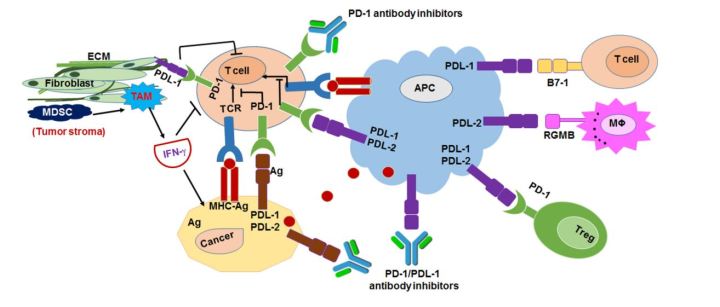
图片来源:Ohaegbulam et al. 2015
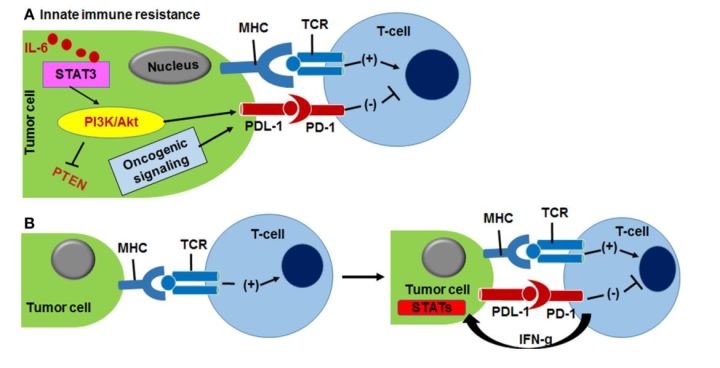
PD-1相关的免疫耐受取决于肿瘤中PD-L1配体的可及性。通过PI3K-Akt激酶的上调或IFN-γ的分泌来监测PD-L1的表达,并且由于PD-L1表达,观察到两种不同类型的免疫耐受,即先天性免疫耐受和适应性免疫耐受。由于先天性免疫耐受,在胶质母细胞瘤中,PD-L1的表达是由与PI3K-Akt致瘤信号激活相关的PTEN的下调所驱动的。PD-1阻滞治疗在前列腺癌中无反应,正是由于PD-L1介导的先天性免疫耐受。
出国看病专家表示,出国看病服务机构了解到某些淋巴瘤和肺癌通过上调信号转导和转录激活因子3(STAT3)和淋巴瘤激酶(ALK)信号阻滞来驱动PD-L1表达。 STAT3的活化通过促炎细胞因子来调节,如IL-6,并且IL-6-STAT3轴被认为是致瘤巨噬细胞极化和免疫抑制中的关键途径之一。在适应性免疫耐受中,一些肿瘤PD-L1的表达是通过来源于肿瘤和肿瘤基质细胞中的促炎性IFN-γ的分泌来诱导,这些IFN-γ可以中和CD8 +细胞毒性T细胞诱导的抗肿瘤免疫应答。
图片来源:Pardoll, 2012
PD-1和PD-L1在抑制效应T细胞功能中起主要作用。临床研究发现,出国看病服务机构了解到阻断PD-1和PD-L1的抗体对许多晚期恶性肿瘤具有可靠作用。针对PD-1和PD-L1靶向治疗是维持效应T细胞功能的有效方式。检查点抑制剂(单克隆抗体mAb)抑制PD-1和PD-L1的相互作用并克服了常规抗癌治疗的缺点。体外和体内研究显示使用抗体阻断PD-1可部分增强T细胞功能。单克隆抗体能够在可耐受的范围内显著降低毒性,同时能够缩小实体肿瘤体积,抑制晚期肿瘤和转移,并提高患者的总生存率。
PD-1和PD-L1是受体-配体系统,在肿瘤微环境中它们彼此连接,从而阻断抗肿瘤的免疫应答。PD-1主要在免疫系统的T细胞上表达,而PD-L1在癌细胞和抗原呈递细胞上。因此,阻断PD-1和PD-L1相互作用的抑制剂可引起T细胞介导的抗肿瘤免疫作用的复活。PD-1和PD-L1抑制剂的有效性还和病人的个体化特征有关,如性别、肿瘤类型、基因的突变和易位,以及肿瘤的转移等。由于肿瘤本质上具有异质性,PD-L1的表达不均匀,因此PD-L1免疫组织化学染色在肿瘤的不同位置也有不同的变化。
免疫治疗的原理和机制大致就介绍这么多,简单地说,通过阻断PD-1和PD-L1的结合从而增强T细胞对肿瘤细胞的识别和攻击就是检查点抑制剂的基本原理。
来自美联医邦的一段话
以上免疫抑制剂的介绍和原理,可以帮助出国看病患者更好地做出明智的医疗决策,美联医邦服务了上千海外国际二诊,美国视频会诊和赴美看病的患者,如有需要请联系我们(400热线:4006162591,电话进来后请告知文章码1219获取专属折扣,客服老师微信:mede1219)
美联医邦海外医疗可协助您参与到美国视频会诊/赴美治疗,详情请阅读下方链接:
https://www.medebound.com/guide/472
美国看病常见问题FAQ
美联医邦提供【病历翻译,医疗签证,医院预约】一条龙服务,为您省时省力,且预约效率更高,可对接到美国医院主任级别专家,费用仅需3万人民币, 请联系我们了解详情。
联系方式:
国内电话热线400-6162591, 电话进来后请告知文章专属码1219获取专属折扣, 或加客服老师微信mede1219立即沟通。
远程会诊|出国成功案例:
安德森会诊案例—晚期胰腺癌赴美安德森治疗为何仍需远程会诊?
赴美面诊美国儿科神经罕见病专家获取美国新药
赴美就医:2023年机构选择和费用
「 MD安德森癌症中心口腔癌治疗案例 」 「 MD安德森癌症中心黑色素瘤治疗案例 」 「 MD安德森癌症中心肺癌治疗案例 」 「 MD安德森癌症中心鼻咽治疗案例 」 「 MD安德森癌症中心肠癌肝癌治疗案例 」
免责声明:本文无意影响或改变您的主治医生提供的医疗服务。 请不要在没有先咨询您的主治医疗服务提供者的情况下对您的治疗做出改变。 本文不用于诊断或治疗疾病,出国看病服务机构了解到也不影响治疗方案。 美联医邦会尽最大努力编辑和更新本页面的信息,但是我们无法保证本页医药信息的精确性和完整性。
本文由美国美联医邦Medebound编辑原创,未经美联医邦允许,不得转载,违者必究。 美国美联医邦借助其30年历史的美国顶级名医网络,用便捷通道帮助国内患者接触到世界先进治疗方法,开展美国肿瘤罕见病名医视频咨询,出国就医和新药绿通,为生命续航。 电话:4006162591,微信公众号:搜索“美联医邦”。
美国美联医邦Medebound HEALTH 是一家创始在美国,总部位于纽约,并在大陆和香港设有分部的国际医疗公司。 董事会由资深的美国医院领导组成。 纽约医学院前院长克鲁力博士担任美联医邦董事和秘书长; 纽约五所医院包括纽约最大医院长老会医院董事卡思先生担任美联医邦董事; 哈佛大学医学院教授,飞利浦全球家庭医疗前首席医疗官维特博士 担任美联医邦独立董事。 我们致力于帮助世界有疑难重疾患者对接到美国顶级医疗资源,专注于开展美国肿瘤罕见病名医的第二诊疗意见,视频咨询,出国就医和美国最新药物申请。 至今美联医邦已经签约中国保险集团总部包括中国平安,泰康,太平人寿等,服务覆盖数百万保险人群。










 美联医邦
美联医邦